Viagra gibt es mittlerweile nicht nur als Original, sondern auch in Form von Generika. Diese enthalten denselben Wirkstoff Sildenafil. Patienten suchen deshalb nach viagra generika schweiz, um ein günstigeres Präparat zu finden. Unterschiede bestehen oft nur in Verpackung und Preis.
Osteoporosi
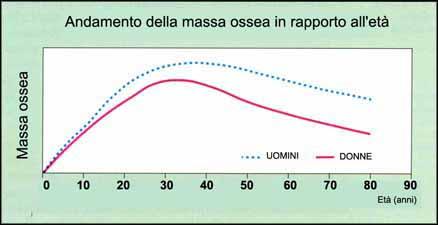
Il nostro scheletro
Contrariamente alle apparenze, anche il nostro scheletro, con le sue 203 ossa fra grandi e piccole, è una parte "viva" del nostro corpo. Basta osservare i cambiamenti che esso subisce nel corso della vita. Dalla nascita fino ai vent'anni circa lo scheletro cresce e si sviluppa. Le ossa aumentano di peso e di volume mentre assumono la loro forma adulta
definitiva. La massa ossea aumenta.
Alla fase di crescita segue una fase di consolidamento, che può arrivare fino ai 25-30 anni di età.
Lo scheletro, senza più crescere, si irrobustisce ulteriormente raggiungendo il cosiddetto picco di
massa ossea, cioé il livello massimo di contenuto di minerali.
Più avanti, anche l'osso perderà lo smalto della giovinezza, e inizierà una lenta perdita di minerali
scheletrici.
Se il punto di partenza era un picco di massa ossea elevato, e se si prendono le corrette misure di
prevenzione, si potrà arrivare a tarda età mantenendo una massa ossea nei limiti della norma. Se
invece si scende al di sotto di questi limiti, si ha la cosiddetta osteopenia (carenza ossea). E se si
scende ancora più in basso si può arrivare al livello dell' osteoporosi (porosità ossea), che implica
un aumentato rischio di fratture.
Le donne, ad ogni età, hanno un valore di massa ossea inferiore a quello degli uomini. E questo è
uno dei motivi per cui esse sono più degli uomini a rischio di osteoporosi.
Diversi tipi di ossa
Le ossa sono di varie forme e dimensioni, e ogni osso è modellato in rapporto alla sua funzione
specifica. Le ossa si classificano in tre gruppi: ossa piatte, ossa lunghe e ossa corte.
Facciamo solo qualche esempio.
Le ossa del cranio sono ossa piatte, saldamente unite fra loro per racchiudere e proteggere organi
essenziali come il cervello e il cervelletto. Le ossa degli arti sono ossa lunghe, di forma cilindrica,
con speciali protuberanze per l'ancoraggio dei tendini (e tramite essi, dei muscoli). Le ossa del
polso sono ossa corte, articolate fra loro in modo da permettere l'estrema mobilità della mano
rispetto all'avambraccio. Anche le 33 vertebre che compongono la colonna vertebrale, e che,
incastrate una sull'altra, costituiscono l'asse portante del nostro corpo, sono ossa corte.
Le ossa sono tutte connesse fra loro, e queste connessioni sono dette articolazioni. Ci sono
articolazioni fisse (p.es. quelle che tengono assieme le ossa del cranio o del bacino), che non
permettono il movimento reciproco delle ossa, e articolazioni mobili (p.es. spalla, gomito, polso,
dita.), in cui le ossa sono libere di muoversi e sono mantenute in posizione da robusti legamenti
fibrosi. A livello delle articolazioni mobili, le ossa hanno superfici di contatto reciproco rivestite di
cartilagine per minimizzare gli attriti, e modellate in modo da permettere certi tipi di movimento (ma
non altri).
Il tessuto osseo
Tutti i tessuti viventi sono in generale
composti - semplificando un po' - di cellule, sostanze intercellulari
(fibre collagene, mucopolisaccaridi, ecc.) e fluidi interstiziali (acqua e sostanze
disciolte nell'acqua).
Il tessuto osseo è un tessuto un po' particolare. Infatti, solo in piccola parte è
composto di cellule viventi e sostanza organica, e contiene pochissimi fluidi
interstiziali. La maggior parte della massa ossea è costituita da sali minerali
(soprattutto fosfati di calcio), depositati su una complessa struttura proteica (matrice proteica, costituita principalmente da fibre collagene). Il valore della massa ossea (più precisamente si dovrebbe dire massa minerale ossea) è il miglior indice della robustezza dello scheletro. In sintesi, possiamo vedere l'osso come costituito da tre componenti:
1) la componente minerale, di per sé inerte, costituita essenzialmente da cristalli di fosfati di calcio
e, in quantità molto minore, da altri minerali. Essa dà all'osso la sua robustezza, e quindi la sua capacità di sostenere il corpo.
2) la componente organica, che comprende la rete di grandi molecole proteiche (matrice) su cui si
depositano i sali minerali.
la componente cellulare, costituita dalle cellule specializzate, osteoblasti e osteoclasti, che
lavorano incessantemente a controllare e mantenere il giusto livello di mineralizzazione delle
ossa. Queste cellule continuamente riassorbono e ricostruiscono le componenti strutturali
dell'osso (organiche e minerali) nel processo di rimodellamento osseo, un processo che va
avanti ogni giorno
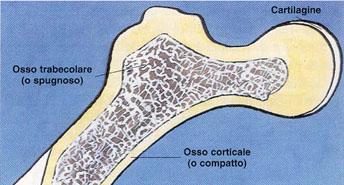
La struttura dell'osso
Più o meno sappiamo tutti com'è fatto un osso. La parte esterna è piuttosto liscia e molto dura (osso compatto), mentre all'interno c'è una complicata struttura simile a una spugna (osso trabecolare o spugnoso), una rete di delicate trabecole collegate tra loro che delimitano piccole cavità contenenti il midollo osseo (l'organo che provvede al rinnovo delle cellule del sangue).
In realtà, a seconda delle ossa, prevale la parte compatta esterna o la parte trabecolare interna. La prima è più importante nelle ossa lunghe, come il femore o l'omero, mentre la seconda è più abbondante nelle ossa piatte, come quelle del cranio o del bacino, e nelle ossa corte, come le vertebre e le ossa del polso. L'osso spugnoso non solo rende le ossa più leggere, ma anche, grazie alla sua complessa architettura trabecolare, le rende più elastiche e meno fragili: nell'osteoporosi, l'aumento di fragilità non è tanto dovuta all'assottigliamento dell'osso corticale, quanto alla perdita e alla rarefazione delle trabecole dell'osso spugnoso, che fa diventare l'osso un po' troppo "vuoto" e quindi strutturalmente più debole del normale.
Le varie ossa - a seconda del tipo e della funzione - contengono una percentuale diversa di osso compatto e osso spugnoso. Le ossa lunghe, come il femore o l'omero, sono formate per lo più da osso corticale molto spesso, tranne verso le estremità, dove prevale l'osso trabecolare. Nelle ossa piatte, come quelle del cranio o del bacino, e nelle ossa corte, come le vertebre, è invece più abbondante l'osso trabecolare, mentre l'osso corticale è solo uno strato sottile.
Le cellule dell'osso e il loro lavoro
Le cellule dell'osso sono di diversi tipi, un po' come operai di diversa specializzazione. Esse sono continuamente al lavoro, lungo tutto l'arco della vita. Ci sono cellule (osteoclasti) che qua e là demoliscono piccole aree di osso vecchio, e altre cellule (osteoblasti) che provvedono a riempire questi "buchi" con osso nuovo. Questo processo si chiama rimodellamento osseo.
Il rimodellamento osseo
Il rimodellamento osseo è il processo con cui le ossa si adattano alle diverse fasi della vita e alle
diverse esigenze dell'organismo. Per tutta la nostra vita, cioè, l'osso continua a essere "rinnovato",
attraverso un ciclo incessante di riassorbimento (distruzione di osso vecchio) e rideposizione
(creazione di osso nuovo) dei suoi sali minerali.
Da giovani si costruisce molto di più osso di quanto se ne demolisce: è il momento della crescita e
dello sviluppo. In questa fase la massa ossea aumenta.
In seguito, nella prima fase della vita adulta, il processo di rimodellamento è in equilibrio: la massa
ossea si mantiene costante perché l'osso nuovo che si deposita va a sostituire completamente
quello riassorbito. Nella tarda maturità, l'osso che si riassorbe tende a essere un po' più di quello
che si riforma. Inizia così la fase della vita in cui si va incontro a una lenta perdita di minerali
scheletrici. Di conseguenza, la massa ossea tende a diminuire. Entro certi limiti, questo è un
fenomeno fisiologico. Se il picco raggiunto in gioventù è alto, e se la perdita è lenta, non bisogna
preoccuparsi oltre misura. I problemi nascono per chi può contare su un capitale osseo iniziale
(picco di massa ossea) non elevato, o su chi perde minerali dall'osso a una velocità anormalmente
elevata. O peggio, entrambe le cose insieme. Come abbiamo già detto, una perdita elevata di
massa ossea si chiama osteopenia, e una così elevata da diventare patologica - con un rischio di
fratture più alto del normale - si chiama osteoporosi.
In qualunque periodo della vita, il rimodellamento osseo è influenzato da tutte le attività che comportano lavoro fisico e sostegno del peso del corpo. Chi ha un corpo robusto, cammina molto, lavora molto in piedi, dà all'osso forti sollecitazioni (pensiamo per esempio a un contadino o a uno sportivo, ma anche a una persona semplicemente sovrappeso), svilupperà un osso più sano e forte di chi è di corporatura esile e fa una vita molto sedentaria.
Fattori fisiologici che agiscono sulla formazione / riassorbimento
dell'osso
Favoriscono la formazione netta di osso
(formazione > riassorbimento)
- attività fisica con carico del peso del corpo (es. camminare)
- normali livelli di ormoni sessuali (estrogeni e testosterone)
- ormone della crescita
- normale attività delle paratiroidi
- normale attività tiroidea
Favoriscono il riassorbimento netto di osso
(formazione < riassorbimento)
- immobilizzazione a letto, attività fisica ridotta
- bassi livelli di ormoni sessuali (menopausa!)
- eccessiva produzione di ormoni corticosteroidi; terapia cortisonica cronica
- eccessiva secrezione di paratormone (stimolata da calcemia bassa o acidosi)
- eccesso di attività tiroidea
La massa ossea
Si parla di massa minerale ossea (in genere abbreviato in massa ossea) o contenuto minerale
osseo per riferirci alla quantità di minerali contenuti nel nostro scheletro.
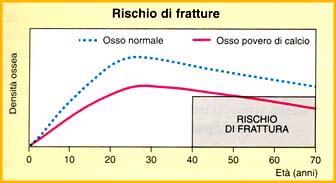
In linea di massima, si può dire che più la massa ossea è alta, più l'osso è robusto. Viceversa, più
la massa ossea è bassa, più è alto il rischio di fratture. Per esempio, si calcola che in una donna di
50 anni con massa ossea normale e con normali prospettive di vita, il rischio di avere in futuro una
frattura da osteoporosi è del 13%. Se la sua massa ossea è bassa il rischio si raddoppia, e se ha
una franca osteoporosi quasi si quadruplica, arrivando al 50%.
La massa ossea è ciò che viene misurato con la mineralometria ossea computerizzata MOC.
Valutare in termini quantitativi la componente minerale dell'osso (e la sua variazione nel tempo)
permette di diagnosticare la presenza o meno di osteoporosi, e il rischio di svilupparla in futuro.
La crescita e il picco di massa ossea Il periodo di massima acquisizione di massa ossea va
dagli 11 ai 18 anni: durante questo periodo di rapida crescita un ragazzo o una ragazza
accumulano circa il 50% della loro massa ossea adulta. La massa ossea che si raggiunge a 20
anni è all'incirca il 90% del valore massimo che si raggiungerà in seguito. Il restante 10% si
aggiunge fra i 20 e i 30 anni, in cui ovviamente il ritmo di accumulo minerali è assai meno intenso.
Abbiamo già detto che il valore massimo di massa ossea che abbiamo raggiunto intorno ai 25-30
anni è chiamato picco di massa ossea. Esso è un valore cruciale per determinare il rischio
individuale di osteoporosi, dato che in seguito la massa ossea più o meno lentamente è destinata
a diminuire.
Fattori che determinano il "picco" di massa ossea effettivamente raggiunto
fattori genetici (sesso, razza, ecc.)
attività fisica
dieta corretta (apporto di calcio!)
normale metabolismo vitamina D
Più alto il picco raggiunto, più difficile sarà scendere fino al livello dell'osteoporosi. Un conto è
perdere calcio partendo da una quota iniziale, poniamo, pari a 100; un altro conto è cominciare a perdere calcio partendo da quota 50. Se la soglia di rischio per le fratture (osteoporosi) è 20, è chiaro che chi parte da un valore basso ci arriverà molto prima, mentre chi parte da un livello molto alto potrebbe anche non arrivarci mai. Ed è anche chiaro perché l'allungamento della vita ha portato a
un così grande aumento dei casi di osteoporosi: perché ci sono a disposizione molti più anni per perdere calcio dall'osso.
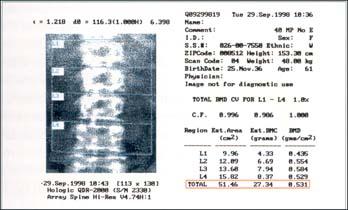
La Mineralometria Ossea Computerizzata (MOC) con tecnica DXA (Dual X-ray Absorptiometry) è
l'esame che misura la massa ossea (o densità minerale ossea), cioè la quantità di minerali
(espressa in grammi) contenuti nel nostro scheletro.
L'esame mineralometrico può essere eseguito a livello dell'avambraccio, della colonna lombare,
del femore o dell'intero scheletro. La MOC-DXA utilizza i raggi X, ma la dose di radiazione
utilizzata per l'esame è bassissima, molto minore di quella di una normale radiografia, e
infinitamente minore di quella di una TAC. Pertanto, non ci sono assolutamente problemi a ripetere
la MOC nel tempo.
Solo questo esame permette di fare con precisione la diagnosi di osteopenia (una modesta
demineralizzazione ossea, che costituisce un po' un campanello di allarme) o osteoporosi (una
demineralizzazione ossea più consstente, che comporta il rischio più o meno grave di fratture). In
una persona adulta, la diagnosi si fa esaminando il T-score, cioè valutando di quanto il valore in
esame si differenzia da quello del campione di riferimento (soggetti sani dello stesso sesso e di età
pari a 25-30 anni, ossia esaminati nel momento in cui si raggiunge il picco di massa ossea).
Valori di T-score compresi fra +1 e -1 indicano una mineralizzazione ossea nella norma.
Secondo i criteri dell'Organizzazione Mondiale della Sanità (originariamente riferiti alle donne in
menopausa, ma oggi utilizzati per gli adulti di ambo i sessi), si parla di osteopenia quando il valore
del T-score è inferiore a -1, e di osteoporosi quando il T-score è inferiore a -2.5.
Il valore misurato della massa ossea, in termini assoluti, è solo un'indicazione di massima. E' chiaro che al disopra di certi limiti si può star tranquilli, mentre al disotto di certi altri bisogna subito prendere provvedimenti. Ma quello che è più importante è seguire la sua variazione nel tempo. In certi casi (per esempio in una donna in menopausa che segue una terapia sostitutiva ormonale e che ha in partenza una buona massa ossea) un secondo controllo si potrà fare anche a qualche anno di distanza dal primo. In altri casi, invece, i
controlli dovranno essere più ravvicinati, anche se in genere non ha senso rifare un controllo MOC prima di un anno dal precedente. Fra una MOC e l'altra potrà invece esser utile effettuare altri tipi di esami di controllo sul sangue e sulle urine (tra cui esami specifici - i cosiddetti markers di turnover osseo - che possono aiutare a valutare l'efficacia dei trattamenti in atto per limitare la perdita di massa ossea).
Accesso alla MOC tramite S.S.N.
Altre tecniche di misurazione della massa ossea
Oggi si stanno sviluppando nuove metodiche di valutazione della mineralizzazione ossea per
mezzo di apparecchi a ultrasuoni (ultrasonografia quantitativa o QUS). Si tratta di metodiche molto
interessanti in quanto di rapida e facile esecuzione. Esse sono considerate utili per l'individuazione
in prima battuta dei pazienti "a rischio di osteoporosi", ma non sono ancora in grado di fornire una
misurazione precisa della massa ossea, e pertanto i pazienti riconosciuti come "a rischio"
dovrebbero sottoporsi a ulteriori accertamenti (esame MOC DXA).
La TAC quantitativa ossea (qCT), dato il costo e l'alta dose di radiazioni, va riservata a casi
particolari.
Osteoporosi
Dopo una certa età, una lenta perdita di minerali dall'osso è normale, o meglio fa parte delle numerose modificazioni che il nostro organismo subisce con l'invecchiamento. Se questa perdita è eccessiva e la massa ossea scende al disotto di determinati livelli (o perché per qualche motivo la perdita è più veloce della norma, o perché è continuata troppo a lungo, o perché si è partiti da un capitale di calcio scheletrico ridotto), allora si può arrivare all'osteoporosi. Un momento critico per le donne arriva con la menopausa, tanto più se precoce o chirurgica. In assenza di precauzioni e di cure, spesso una donna di 70 anni - un'età che oggi non appare più tanto avanzata - si trova ad aver perso senza accorgersene il 30% e più della sua massa ossea adulta. Se consideriamo che le donne hanno in partenza una massa ossea minore rispetto agli uomini, aggiungiamo gli effetti della menopausa e la maggior durata della vita, ecco la prima spiegazione del perché l'osteoporosi colpisce
soprattutto le donne: 1 donna su 4 contro 1 uomo su 10.
La malattia
L'osteoporosi si definisce come "una malattia sistemica dello scheletro, caratterizzata da ridotta massa minerale e deterioramento microstrutturale del tessuto osseo, con conseguente aumento della fragilità dell'osso e maggior rischio di fratture".
Si calcola che, nel mondo, circa 200 milioni di persone siano attualmente affette da osteoporosi. Solo in Europa, USA e Giappone, l'osteoporosi colpisce più di 75 milioni di persone. La tendenza all'allungamento della vita media e all'invecchiamento delle popolazioni, in mancanza di seri interventi di prevenzione, determinerà nei prossimi decenni un significativo aumento dei casi. Attualmente, ogni anno, in Europa e USA, si verificano più di 2.3 milioni di fratture da osteoporosi. Nel 1990, nel mondo, le fratture di femore sono state stimate a 1,6 milioni; per il 2050 se ne attendono 6,3 milioni.
Per l'Italia mancano ancora dati precisi sul numero di persone realmente affette da osteoporosi, ma si valuta che nel 1990 l'osteoporosi abbia causato circa 100.000 fratture di polso e 60.000 fratture di femore. Non sono quantificabili le fratture vertebrali, che in genere non passano dal "pronto soccorso" degli ospedali e non vengono quindi rilevate a fini statistici.
Come si arriva all'osteoporosi
In sintesi, il rischio di arrivare all'osteoporosi è il risultato della combinazione di tre fattori:
- il "picco di massa ossea", il nostro capitale osseo raggiunto intorno ai 25-30 anni - la velocità con cui procede la perdita di massa ossea che inevitabilmente inizia fra i 40 e i 50 anni, e in
particolare, per le donne, a partire dalla menopausa
- la durata di questa perdita, che ovviamente dipende dalla longevità dell'individuo, e che nelle donne è tanto
più lunga quanto più la menopausa è precoce
Un corretto programma di prevenzione - basato su una dieta corretta e su una regolare attività fisica - può modificare sensibilmente i primi due fattori, e quindi ridurre significativamente i rischi di fratture ossee da osteoporosi.
I segni e i sintomi dell'osteoporosi
L'osteoporosi è una malattia difficile da riconoscere: il più delle volte non dà nessun segno di sè.
Per questo è stata definita il "ladro silenzioso", perché ruba per anni, senza farsene accorgere, il
calcio del nostro osso. Solo in alcuni casi, l'osteoporosi può accompagnarsi a dolore osseo, che
però spesso si confonde e si associa con i dolori determinati da un'altra malattia molto frequente negli anziani, l'artrosi. Il dolore legato a queste due patologie ha comunque una certa specificità.
Purtroppo, nella maggior parte dei casi, l'osteoporosi non dà nessun segnale premonitore, e si
manifesta improvvisamente con una delle tipiche fratture "da fragilità ossea" dell'anziano: fratture
di polso, coste, vertebre o femore a seguito di traumi anche molto lievi e banali.
Per evitare una brutta sorpresa di questo genere, a una certa età bisogna valutare la propensione
individuale all'osteoporosi analizzando i propri "fattori di rischio". In particolare, è
importantissimo che questa valutazione venga fatta, meglio se con l'aiuto del medico, da tutte le
donne che si avvicinano alla menopausa, specie se non si sono mai preoccupate prima della
prevenzione dell'osteoporosi.
In presenza di fattori di rischio, o comunque verso i 65 anni, è consigliabile sottoporsi a una
misurazione della propria "densità minerale ossea" con la MOC.
La MOC DXA è oggi considerata l'esame più attendibile per la diagnosi di osteoporosi.
Le fratture da osteoporosi
Le fratture da osteoporosi sono più frequenti in certi distretti scheletrici.
Spesso il primo allarme viene dato da una frattura del polso, la cosiddetta frattura di Colles, a
seguito di una banalissima caduta. Nell'età avanzata, sono soprattutto due i punti delicati, le
vertebre e il femore. Altre sedi di fratture da osteoporosi sono la spalla (omero) e le coste.
Le fratture vertebrali si manifestano con un dolore improvviso e violento alla schiena, che di solito,
specie se a livello lombare, rende difficili o quasi impossibili i movimenti. Le fratture vertebrali
possono avvenire non solo a seguito di una caduta, ma spesso anche facendo movimenti scorretti,
come il classico piegamento in avanti per raccogliere un oggetto, o sollevando un peso, p.es.
prendendo in braccio un nipotino. E' importante capire che si tratta di una frattura, e non di un
banale "mal di schiena" per altre cause, per cui, appena possibile, si dovrà fare un esame
radiologico della colonna vertebrale. Fino a pochi anni fa, l'unico modo di "curare" le fratture
vertebrali era il riposo - a letto nei primi giorni, poi in poltrona. Oggi esiste anche la possibilità di
intervenire chirurgicamente, con due tecniche diverse chiamate "vertebroplastica e
cifoplastica". Si tratta di interventi volti a stabilizzare la situazione, soprattutto al fine di ridurre il
dolore. Tuttavia la possibilità di intervenire va valutata caso per caso.
In assenza di intervento chirurgico, la fase acuta, quella in cui il dolore impedisce una vita normale,
dura in genere da due a quattro settimane, durante le quali il medico prescriverà degli analgesici
adatti per ridurre il dolore a livelli sopportabili. In molti casi, purtroppo, le fratture vertebrali lasciano
un corredo di dolori cronici che in genere si manifestano quando il paziente si affatica o sta troppo
a lungo in posizione eretta. In alcuni casi, saranno utili corsetti e altri presidi ortopedici. Purtroppo
le fratture vertebrali spesso si ripetono a distanza di tempo, e possono quindi causare una perdita
anche di parecchi centimetri di altezza.
Le fratture di femore sono fortunatamente più rare, ma molto più temibili. Di solito colpiscono
persone più anziane, con un'osteoporosi avanzata e magari non riconosciuta e non curata, a
seguito di una caduta. Richiedono il ricovero in ospedale, un intervento chirurgico, e una più o
meno lunga riabilitazione. Molte persone, anche molto anziane, riescono a superare brillantemente
anche una frattura di femore e in pochi mesi riprendono la vita di prima. Altre non sono così
fortunate e non recuperano più la piena indipendenza. Alcune, purtroppo, vanno incontro a
complicazioni varie a causa della lunga degenza a letto, e non è neppure trascurabile la mortalità.
Il recupero è in genere tanto migliore quanto più la persona, prima della frattura, faceva una vita
attiva ed era in buone condizioni fisiche e mentali. Il desiderio di guarire e la buona volontà
nell'impegnarsi nella riabilitazione sono elementi importantissimi per una buona ripresa dopo una
frattura di femore.
In presenza di osteoporosi e in particolare dopo una frattura
Una persona con osteoporosi, in particolare se ha già avuto fratture, deve assolutamente seguire
(o iniziare) una terapia farmacologica per l'osteoporosi: in questi casi, la semplice alimentazione
ricca di calcio, l'attività fisica, e magari un supplemento di calcio e/o vitamina D non bastano più.
Occorre aggiungere a questi mezzi di prevenzione, che restano comunque validi, anche un
farmaco capace di riportare il metabolismo osseo verso l'equilibrio fra riassorbimento e
formazione.
Tipi diversi di osteoporosi
L'osteoporosi classica è una malattia della terza età, e in primo luogo delle donne in menopausa. Si parla quindi di osteoporosi senile o meglio, nella donna, di osteoporosi post-menopausale. L'osteoporosi post-menopausale è legata essenzialmente alla brusca caduta del livello degli estrogeni, gli ormoni sessuali necessari, tra l'altro, per il normale metabolismo osseo. Nel sesso maschile, l'osteoporosi senile colpisce più tardivamente sia perché l'uomo ha in genere in partenza, per motivi genetici, un osso più robusto e più ricco di calcio, sia perché la caduta degli ormoni sessuali maschili è molto più lenta e graduale. Esistono anche forme di osteoporosi giovanile, che possono colpire a tutte le età. Queste forme sono decisamente meno frequenti dell'osteoporosi post-menopausale. Nel caso di riscontro casuale di osteoporosi in una persona sotto i 50 anni, per esempio a seguito di una frattura, si tratta per lo più di una osteoporosi secondaria ad un'altra causa. Pertanto si deve cercare la possibile causa della perdita di calcio dall'osso. Esistono molte forme secondarie di osteoporosi, dovute a malattie di diversa natura: riconosciuta e messa sotto controllo la malattia primaria che ne è la causa, spesso l'osteoporosi può risolversi, dato che nelle persone più giovani esistono buone possibilità di recupero della massa ossea. Le malattie che più spesso sono causa di osteoporosi, non sempre facilmente riconosciute perché povere di segni e sintomi rilevanti, sono: - le malattie che determinano malassorbimento intestinale, e che quindi non permettono un assorbimento ottimale del calcio alimentare (malattia di Crohn, celiachia, ecc.); - le malattie che portano a una ridotta assunzione alimentare di calcio, come l'anoressia nervosa; - le malattie che determinano, in generale, un cattivo stato metabolico, e che in particolare determinano un'insufficiente disponibilità dei metaboliti attivi della vitamina D (malattie ostruttive respiratorie croniche, insufficienza renale cronica, epatopatie croniche); - le malattie che determinano una continua perdita di calcio con l'urina (ipercalciuria idiopatica); - le alterazioni del sistema endocrino che interferiscono con la regolazione del metabolismo osseo (ipogonadismi; menopausa precoce (prima dei 45 anni); amenorree prolungate (>1 anno); iperparatiroidismo; ipertiroidismo; malattia di Cushing; iperprolattinemia); - malattie che interessano direttamente l'osso, come il mieloma multiplo; - malattie che riducono fortemente l'attività fisica o che richiedono lunghe cure a base di cortisone (artrite reumatoide, lupus eritematosus sistemico, fibrosi cistica, distrofia muscolare, trapianti d'organo, ecc.); - malattie che richiedono l'uso cronico di particolari farmaci (oltre ai corticosteroidi già citati: eparina, anticonvulsivanti, antiacidi).
Ripetiamo: una corretta diagnosi e la consapevolezza che certe malattie possono direttamente o indirettamente causare osteoporosi permettono di prendere tutte le misure necessarie per prevenire o ridurre i danni subiti dall'osso. Per esempio, in molti casi in cui si diagnostica la celiachia solo dopo aver scoperto più o meno casualmente un'osteoporosi, la semplice introduzione di una dieta priva di glutine può determinare in poco tempo un importante miglioramento della situazione ossea.
Osteomalacia e rachitismo
L'osteomalacia è una malattia dello scheletro caratterizzata da una difettosa mineralizzazione, con accumulo nell'osso di matrice (osteoide) non mineralizzata. L'osso così formato è più debole e
molle del normale e subisce deformazioni con il carico (p.es. gambe incurvate). Il termine
osteomalacia si riferisce alla malattia dell'adulto, che si sviluppa dopo la fine della crescita. Il
termine rachitismo è usato invece per lo scheletro ancora in crescita, in cui il difetto di
mineralizzazione riguarda sia l'osso sia la cartilagine epifisaria.
La forma più frequente di osteomalacia è dovuta ad una carenza di vitamina D, che può essere
determinata da ridotta produzione nell'organismo, malassorbimento, malattie epatiche, terapie
anticonvulsivanti croniche. Meno frequenti sono le osteomalacie dovute a alterato metabolismo
della vitamina D, resistenza all'azione della vitamina D, ipofosforemia e ipofosfatasia.
Mineralizzazione ossea
Per mineralizzare l'osteoide in modo soddisfacente, lo scheletro richiede una quantità adeguata di minerali (principalmente calcio e fosforo), normali livelli plasmatici dei metaboliti della vitamina D e normale attività degli osteoblasti (le cellule che formano osso nuovo). Nel normale processo di rimodellamento osseo, gli osteoblasti depositano osteoide (la matrice organica dell'osso, costituita per lo più da collagene di tipo I) in una piccola parte di osseo prima erosa dagli osteoclasti (le cellule che distruggono l'osso vecchio). Gli stessi osteoblasti favoriscono la precipitazione di calcio e fosforo sull'osteoide, provocandone la mineralizzazione. Una carenza di calcio e fosforo o un livello inadeguato di vitamina D impedisce il normale processo di mineralizzazione e determina la comparsa di osteomalacia.
Segni e sintomi
Le manifestazioni cliniche dell'osteomalacia possono variare, ma sono simili nelle varie forme, e sono: dolore muscolare e osseo, deformità e fratture ossee, debolezza muscolare e ipocalcemia. Nell'infanzia il rachitismo è caratterizzato da allargamento delle epifisi e ritardo nell'accrescimento. Negli stadi iniziali l'osteomalacia può non essere riconosciuta perché i sintomi sono spesso molto sfumati. Il paziente può riferire dolori aumentati dalla contrazione muscolare, ma anche a riposo. Successivamente l'osso non mineralizzato, più molle e elastico, può andare incontro a deformazioni, con comparsa di cifosi (incurvamento della schiena), scoliosi, incurvamento delle ossa lunghe (tipiche le gambe curve). Si può avere una sofferenza dei muscoli prossimali, che provoca un'andatura ondeggiante, e che determina difficoltà ad alzarsi da una sedia o a salire una scala. Si possono verificare fratture per piccoli traumi o spontanee, e schiacciamenti vertebrali. I bambini affetti da rachitismo presentano riduzione dell'altezza e incurvatura delle gambe. Nelle forme più gravi, oggi rare, spesso i bambini sono molto deboli, fino all'impossibilità di alzarsi e di camminare.
Diagnosi
Anche nell'osteomalacia (come nell'osteoporosi) la densità ossea è ridotta. Nelle forme più gravi si possono vedere con le radiografie delle zone più trasparenti (decalcificate) perpendicolari alla superficie ossea, dette strie di Looser, circondate da osso più denso. Queste alterazioni sono più frequenti a livello del femore, dell'omero, del bacino e delle coste. Ci possono essere anche piccole fratture, soprattutto a livello delle parti che sopportano il carico (gambe, piedi).
Laboratorio
A seconda del tipo di osteomalacia, si possono trovare delle alterazioni nei valori di calcio, fosforo e della vitamina D (25-idrossi vitamina D e 1,25-diidrossi vitamina D). Nelle osteomalacie da carenza di vitamina D, i livelli di calcio sono normali o poco ridotti, mentre quelli di fosforo e di 25-idrossi vitamina D lo sono di più. Se il deficit di vitamina D è più marcato, la calcemia si riduce ulteriormente e si alzano i livelli di paratormone (iperparatiroidismo secondario). I livelli di fosfatasi alcalina sono per lo più elevati.
FORME SPECIFICHE
1. Osteomalacia da carenza di vitamina D
Insufficiente produzione o apporto dietetico
La ridotta esposizione alla luce solare, la ridotta capacità di produzione cutanea, il ridotto
assorbimento, e lo scarso apporto dietetico sono tutti fattori che provocano un deficit di vitamina D.
Sono più a rischio gli anziani che vivono in case di riposo, o che sono ricoverati a lungo, i neonati
nati in inverno nelle regioni nordiche (se non viene seguita la normale profilassi con vitamina D), e
gli immigrati, che spesso seguono una dieta molto carente.
Malassorbimento
L'osteomalacia da carenza di vitamina D si verifica anche nelle varie forme di malassorbimento
(celiachia, enteriti regionali, bypass e resezioni intestinali). In questi casi oltre al ridotto
assorbimento della vitamina D si aggiunge quello di calcio e fosforo. In particolare, i pazienti con
celiachia misconosciuta possono manifestare chiari segni di osteomalacia. Il trattamento della
celiachia (dieta priva di glutine) corregge in parte anche l'osteomalacia.
Epatopatie
Le malattie epatiche (in particolare la cirrosi biliare primitiva), determinano una carenza di vitamina
D per il ridotto assorbimento della stessa, per l'alterato metabolismo epatico (minore produzione
del 25-idrossi vitamina D).
Terapia dell'osteomalacia da carenza di vitamina D
Il trattamento dell'osteomalacia da carenza o da malassorbimento si basa sulla somministrazione
della vitamina D. Attualmente sono disponibili sia le forme di vitamina D nativa sia i metaboliti attivi
(calcifediolo, calcitriolo o alfacalcidolo). La scelta del tipo di vitamina D e del dosaggio dipendono
dalla causa dell'osteomalacia e dalla sua gravità. Il trattamento dell'osteomalacia determina la
scomparsa della miopatia prossimale e dei sintomi legati all'ipocalcemia in poche settimane,
mentre i dolori ossei spariscono più lentamente. Ricordiamo che la somministrazione di dosi
terapeutiche di vitamina D o dei suoi metaboliti necessita di attenti controlli clinico-laboratoristici
(per evitare i rischi di ipercalciuria e ipercalcemia) e di costanti aggiustamenti dei dosaggi.
2. Osteomalacia da difetti nel metabolismo o nell'attività della Vitamina
D
Difettosa sintesi 25-idrossi vitamina D
Estremamente rara, legata a difetti ereditari della 25-idrossilasi epatica. Sono stati descritti pochi
casi, solo in bambini.
Difettosa sintesi 1,25-diidrossi vitamina D
Insufficienza renale cronica
Nell'insufficienza renale cronica il rene perde la capacità di trasformare la 25-idrossi vitamina D in
1,25-diidrossi vitamina D.
Rachitismo vitamino D-dipendente di tipo I
Si tratta di una grave forma di rachitismo precoce (dai primi anni di vita), con miopatia e difetti nella
dentizione. E' relativamente frequente in Canada. È una malattia ereditaria (autosomica
recessiva), con ridotta sintesi di 1,25-diidrossi vitamina D.
3. Osteomalacia da difettosa attività dei recettori vitamina D
Rachitismo vitamino D-dipendente di tipo II
Si tratta di una forma ereditaria (autosomica recessiva), più frequente nell'area mediterranea. Il
difetto consiste in alterazioni dei recettori dell'1,25-diidrossi vitamina D, che non sono più in grado
di funzionare normalmente. I bambini sono normali alla nascita, ma verso i due anni compaiono
alterazioni ossee e ipocalcemia, con elevati livelli di 1,25-diidrossi vitamina D.
4. Osteomalacia da ipofosforemia
L'ipofosforemia si osserva nelle carenze di vitamina D, sia per un ridotto assorbimento sia per l'iperparatiroidismo secondario. Tuttavia, in certe forme, essa è il difetto primitivo che conduce all'osteomalacia, pur in presenza di normali livelli di calcio.
Carenze di fosforo
Sono infrequenti, tranne che nei casi di nutrizione parenterale, soprattutto nei bambini.
Rachitismo ipofosforemico vitamino D-resistente
Si tratta di una forma di rachitismo con ipofosforemia, bassa statura e le tipiche deformazioni delle
ossa lunghe delle gambe si evidenziano con il carico. Si tratta di una malattia ereditaria dominante
legata al sesso (cromosoma X). L'ipofosforemia si determinerebbe per un'alterazione del trasporto
tubulare del fosforo.
5. Osteomalacia da cancro (osteomalacia oncogena)
L'osteomalacia può accompagnare, o anche precedere di molto tempo, la comparsa di tumori (per lo più mesenchimali, ma anche carcinomi mammari, polmonari, prostatici, mieloma e leucemie). Dolori ossei, fratture e profonda debolezza muscolare sono piuttosto frequenti. L'ipofosforemia è dovuta a eccessive perdite renali. I livelli di 25-idrossi vitamina D sono normali, mentre quelli di 1,25-diidrossi vitamina D possono essere francamente ridotti. La rimozione del tumore porta a una completa risoluzione del quadro osseo.
6. Osteomalacia da farmaci
Anticonvulsivanti
I farmaci anticonvulsivanti (fenobarbital, fenitoina, carbamazepina) determinano una minore
produzione di 25-idrossi vitamina D a livello del fegato.
Fluoruri
I fluoruri ad alte dosi, in assenza di adeguata supplementazione con calcio e vitamina D, inducono
la comparsa di una alterata mineralizzazione ossea, interferendo con la formazione dei cristalli di
idrossiapatite.
L'iperparatiroidismo è una malattia causata da un'eccessiva secrezione di ormone paratiroideo
(detto anche paratormone o PTH) da parte delle ghiandole paratiroidi, quattro piccole ghiandole
endocrine annesse alla ghiandola tiroide.
Le paratiroidi sono ghiandole fondamentali per la regolazione del metabolismo del calcio. Quando esse rilevano una riduzione della calcemia (la concentrazione di calcio nel sangue) rispondono con una secrezione di paratormone, il principale ormone ipercalcemizzante (ossia in grado di aumentare la calcemia). La calcemia deve essere mantenuta entro stretti limiti per assicurare diverse funzioni vitali come la contrazione dei muscoli (compreso il cuore), l'attività nervosa, la coagulazione del sangue. Il paratormone agisce sull'osso, la riserva di calcio dell'organismo, stimolando l'attività degli
osteoclasti e quindi il riassorbimento osseo: la calcemia quindi aumenta a spese dell'osso, che
perde calcio a favore del sangue. Questo processo è del tutto normale, e in condizioni di equilibrio
(cioè con un normale apporto alimentare di calcio e un normale assorbimento intestinale, grazie
all'azione della "vitamina D" ben presto l'osso potrà recuperare il calcio momentaneamente
perduto.
In condizioni patologiche, invece, come nel caso dell'iperparatiroidismo, questo recupero può non
avvenire, e in questo caso l'osso va incontro a una perdita progressiva di calcio, sviluppando a
lungo andare prima osteopenia e poi osteoporosi.
Forme di iperparatiroidismo
Le forme principali di iperparatiroidismo sono due, l'iperpartiroidismo primitivo e quello secondario.
L'iperparatiroidismo primitivo è in genere dovuto alla presenza di un adenoma paratiroideo, cioè
di un tumore benigno che secerne quantità eccessive di ormone. A volte ci può essere
un'eccessiva secrezione di paratormone anche senza la presenza di un vero e proprio adenoma
(per cause genetiche).
L'iperparatiroidismo secondario è invece una risposta delle paratiroidi a una condizione di
ipocalcemia (calcemia inferiore al normale) cronica, come quella che si può verificare nel caso di
un deficit di "vitamina D" (insufficiente sintesi nella pelle per mancanza di esposizione al sole,
oppure gravi malattie epatiche o renali che impediscono l'attivazione della vitamina D).
In casi particolari, dopo un lungo periodo di iperparatiroidismo secondario (come p.es. può
avvenire nell'insufficienza renale cronica di lunga data), le paratiroidi possono perdere la loro
capacità di autoregolazione e si mettono quindi a secernere paratormone indipendentemente dalla
presenza di ipocalcemia. In questi casi (rari) si parla di iperparatiroidismo "terziario".
Le conseguenze dell'iperparatiroidismo
Nei casi lievi, l'iperparatiroidismo è completamente asintomatico e si scopre solo per caso. Se invece l'aumento di calcemia provocato dall'eccesso di paratormone è significativo, si possono avere vari disturbi: debolezza muscolare (braccia e gambe), disturbi digestivi (nausea, vomito, perdita di appetito, dolori addominali, stitichezza), disturbi nervosi (nervosismo, confusione mentale, e nei casi estremi anche delirio, sonnolenza, coma), calcoli renali e relative coliche (per eccesso di escrezione di calcio), e naturalmente alterazioni a carico dell'osso (osteopenia, osteoporosi) e delle articolazioni (calcificazioni e dolori articolari). Livelli estremamente elevati di calcemia possono arrivare a mettere in pericolo la vita.
Diagnosi dell'iperparatiroidismo
La diagnosi di iperparatiroidismo può essere difficile, ed è importante prenderla in considerazione in presenza di certi dati clinici o di laboratorio. Gli esami di laboratorio più utili per la diagnosi sono i livelli di paratormone e di calcio nel sangue. Ulteriori accertamenti possono essere poi effettuati con esami come l'ecografia del collo, la TAC, la scintigrafia e l'angiografia.
Terapia dell'iperparatiroidismo
Nell'iperparatiroidismo primitivo, nei casi gravi, in presenza di sintomi importanti (p.es. ipercalcemia severa) o di complicanze (p.es. calcolosi renale) si può ricorrere all'asportazione chirurgica dell'adenoma paratiroideo. Se invece le alterazioni sono modeste e il paziente non accusa sintomi, l'opportunità dell'intervento chirurgico è discussa. Per controllare l'ipercalcemia in attesa dell'intervento chirurgico, o quando questo non è indicato, possono essere utilizzati i bisfosfonati. Nel caso di iperparatiroidismo secondario a carenze di vitamina D occorre somministrare dose adeguate di vitamina D o di calcifediolo (il metabolita attivato a livello epatico). Nel caso in cui l'iperparatiroidismo sia secondario a malassorbimento intestinale o a deficit alimentari di calcio, il primo intervento deve essere volto a correggere questa situazione. Particolarmente complesso è il
trattamento dell'iperparatiroidismo secondario ad insufficienza renale, che richiede vari provvedimenti terapeutici.
Osteogenesi imperfetta (OI)
L'osteogenesi imperfetta è la più frequente malattia ereditaria del collagene, la proteina
filamentosa che forma la trama della matrice ossea (su cui si depositano i sali di calcio). L'OI è
caratterizzata da osteopenia, fratture ricorrenti e deformità scheletriche.
La sua frequenza è di circa 1 su 10.000 nascite.
La classificazione dell'OI
Ci sono quattro tipi principali di osteogenesi imperfetta.
Le forme più frequenti, e per fortuna anche più lievi, sono quelle di Tipo I. Sono spesso
caratterizzate dalla presenza di sclere blu (la parte bianca degli occhi è cioè di colore azzurrino), e
non compromettono significativamente la crescita. Anche le forme di Tipo IV (in cui le sclere blu
sono presenti solo nella prima infanzia, poi diventano bianche) sono in genere di gravità lieve o
moderata, anche se più spesso si hanno compromissioni della crescita. Molto più gravi sono
invece le forme di Tipo III, in cui si hanno fratture già "in utero" e successivamente si hanno gravi
deformità ossee e compromissione della crescita. Infine, sono addirittura incompatibili con la vita le
forme di Tipo II, in cui si ha aborto o morte poco dopo la nascita.
La malattia può essere ereditata dai genitori oppure può dipendere da nuove mutazioni spontanee. Ovviamente, nel caso di mutazioni spontanee, i genitori sono sani. Nel caso dell'OI di Tipo III - a ereditarietà autosomica recessiva - i genitori possono essere "portatori sani" . Nelle forme I e IV, a ereditarietà autosomica dominante, un soggetto malato che sposa un soggetto sano ha all'incirca una probabilità su 2 di avere un figlio malato.
Alterazioni del collagene
L'OI è determinata da alterazioni dei geni che codificano il collagene. Nei casi meno gravi (tipo I) le mutazioni in genere determinano la produzione di una quantità ridotta di collagene a struttura normale. Nei casi più gravi (tipo II, III, IV) le mutazioni per lo più determinano la produzione di collagene a struttura anomala, che contiene fibrille con struttura alterata o incapaci di legarsi all'idrossiapatite (il sale minerale caratteristico dell'osso).
Manifestazioni cliniche
La grande varietà delle mutazioni determina una grande varietà di quadri clinici: si va dai casi in cui si ha morte in utero per fratture multiple ai casi in cui non si verificano mai fratture e la diagnosi si ha solo sulla base della storia familiare. Il segno più specifico è la frattura, conseguente alla scarsa mineralizzazione dell'osso (osteopenia). Spesso, fra la nascita e la pubertà, i bambini hanno 10 o anche più fratture di vario tipo, soprattutto alle ossa lunghe (braccia e gambe), spesso anche per minimi traumi. Durante l'adolescenza, la frequenza delle fratture tende a ridursi sia nei maschi che nelle femmine. Nelle donne si ha un aumento delle fratture, soprattutto a livello vertebrale, dopo la menopausa. In molti pazienti si hanno sclere di colore blu o grigio, e sono anche frequenti anomalie della dentina (denti di aspetto traslucido e più fragili del normale). Dopo i 40 anni, spesso compare sordità, forse dovuta a fratture degli ossicini dell'orecchio. Nelle forme più gravi si ha bassa statura, scoliosi e deformità toraciche, che predispongono a ripetute infezioni polmonari.
Diagnosi
La diagnosi si basa sulla storia clinica (familiarità) e sullo studio del collagene. È sempre presente una significativa riduzione della massa ossea (che si rileva con la MOC) e si osservano deformità osee dovute alle fratture ricorrenti. La diagnosi prenatale delle forme gravi di OI si può fare con ecografia tra la 14ma e la 18ma settimana di gestazione. Nell'infanzia la diagnosi differenziale è soprattutto con le fratture provocate da violenze e maltrattamenti dei bambini, e inoltre con l'osteoporosi idiopatica giovanile e l'omocistinuria. Nelle età più avanzate con tutte le forme primitive o secondarie di osteopenia e osteoporosi.
Non ci sono terapie mediche risolutive, ma solo di supporto. Tra i farmaci disponibili, i bisfosfonati sembrano i più efficaci e, con le dovute cautele, sono ormai usati anche nei bambini. È fondamentale una buona assistenza ortopedica e fisioterapica per evitare deformità e per ridurre al massimo i periodi di immobilità e il rischio di osteopenia da disuso. La prognosi è buona nel tipo I (la forma più comune). Le conseguenze più gravi sono riscontrate nella forma III. Le cause più frequenti di morte sono i problemi respiratori (infezioni) dovute sia alle deformità della gabbia toracica sia alle fratture costali.
Morbo di Paget osseo
Il morbo di Paget osseo è una delle malattie ossee più frequenti dopo l'osteoporosi: colpisce circa l'1-5% della popolazione dopo i 50 anni, un po' più gli uomini delle donne. La causa è sconosciuta, ma spesso la malattia è ricorrente nell'ambito della famiglia. Si tratta di una alterazione focale (cioè localizzata) del tessuto osseo dovuta a un abnorme aumento del riassorbimento, mediato dagli osteoclasti. Le ossa colpite (sopratutto pelvi, femore, vertebre, cranio e tibia) cambiano forma e dimensioni, mentre il resto dello scheletro resta intatto. Può essere interessato un solo osso (forma monostotica) o più ossa (forma poliostotica). Il morbo di Paget osseo è una malattia a progressione lenta. L'osso colpito perde la normale struttura lamellare e acquista un aspetto ‘intessuto' (woven bone). L'osso perde le sue qualità di resistenza e elasticità e diventa più suscettibile a deformazioni e fratture.
Segni e sintomi
I segni e sintomi più comunemente presenti sono: dolore osseo nella sede interessata e, in circa il 15% dei casi, deformazioni ossee. La zona di osso interessata può essere più calda per l'aumentata vascolarizzazione, e ciò è spesso percepito come fastidioso. Molti pazienti sono del tutto asintomatici, e la malattia viene scoperta accidentalmente da una radiografia o in seguito al riscontro di una persistente elevazione della fosfatasi alcalina plasmatica.
Diagnosi
L'approccio diagnostico consiste nello studio radiologico delle aree colpite e nella scintigrafia ossea, che permette di vedere tutto lo scheletro e individuare tutte le aree interessate dalla malattia. Dal punto di vista del laboratorio sono aumentati tutti i markers del turnover osseo: quello più comunemente misurato è la fosfatasi alcalina.
La terapia punta a ridurre i danni ossei, prevenire le complicanze, e indurre una remissione di lunga durata. Attualmente le terapia di prima scelta si basa sull'impiego dei bisfosfonati (farmaci antiriassorbimento osseo). Sono usati soprattutto alendronato, risedronato, neridronato, clodronato. Questi farmaci si sono mostrati in grado di indurre una riduzione degli indici di turnover osseo in più del 60% dei pazienti con morbo di Paget, in alcuni casi fino alla normalizzazione.
Dopo la terapia occorre seguire l'evoluzione della situazione nel tempo, controllando ogni 6-12 mesi almeno un "marker" osseo.
Malattia di Sudek
E' una sindrome conosciuta con vari nomi, tra cui "Algoneurodistrofia", "Distrofia simpatica riflessa", "Osteoporosi regionale dolorosa". Colpisce per lo più persone al di sotto dei 50 anni, inclusi i bambini, più spesso di sesso femminile. Nei casi più tipici, si manifesta con dolore, spesso molto forte, limitazione dei
movimenti e altri segni e sintomi che sembrerebbero indicare una componente vasomotoria (gonfiore, atrofia dei tessuti). Radiologicamente, spesso si osserva un'osteoporosi localizzata più o meno marcata, che riguarda un singolo osso o più ossa adiacenti. Tuttavia l'osteoporosi è solo una componente della sindrome e non è necessariamente presente. La causa è sconosciuta. Spesso la sindrome compare in seguito a un trauma a un'estremità, e appare come una forma di eccessiva risposta ad esso, con ritardata guarigione. In genere interessa una singola localizzazione all'arto superiore (soprattutto avambraccio distale, polso, mano) o inferiore (soprattutto caviglia o piede). A volte può ripetersi nel tempo in zone diverse ("Osteoporosi regionale migrante"). In genere l'evoluzione è favorevole, con risoluzione in 6-18 mesi. La cura è sintomatica e, se c'è osteoporosi, basata sui bisfosfonati.
Artrite, artrosi e osteoporosi: malattie diverse che a volte vanno insieme
E' importante chiarire il significato di questi termini di uso molto comune, ma spesso interpretati in modo inesatto, perché si tratta di malattie che colpiscono milioni di persone. Mentre l'osteoporosi è una malattia dell'osso, l'artrite e l'artrosi sono malattie delle articolazioni, ossia di quelle complesse strutture che tengono unite fra loro due o più ossa distinte, in genere permettendo che esse eseguano movimenti reciproci con il minimo attrito. Si distinguono le grandi articolazioni (ginocchio, anca, gomito, spalla), e le piccole articolazioni (polso, mano, piede, vertebre.). Le articolazioni sono tenute insieme da un manicotto fibroso, la capsula articolare, e da complesse strutture a nastro (legamenti). La forma dei capi articolari delle ossa determina le possibilità di movimento reciproco, che possono essere più o meno ampie. Per intenderci, pensate ai movimenti possibili dell'articolazione della spalla e a quelli del gomito: la spalla permette movimenti dell'arto superiore praticamente in tutte le direzioni, il gomito si può solo flettere o estendere (piegare o raddrizzare). Le facce articolari delle ossa sono rivestite di un tessuto estremamente levigato ed elastico, la cartilagine articolare, che permette il movimento reciproco delle ossa con il minimo attrito, grazie anche alla continua lubrificazione assicurata dalla membrana sinoviale (una membrana sottilissima che riveste la faccia interna della capsula articolare).
Ogni alterazione o erosione delle facce articolari determina difficoltà e limitazioni nei movimenti, e soprattutto dolore. Partiamo dalla condizione meno frequente. Il termine artrite indica una malattia articolare determinata da un processo infiammatorio. Le artriti acute (a parte il reumatismo articolare acuto) sono assai poco frequenti. Fra le artriti croniche, la forma più comune è l'artrite reumatoide. Si tratta di una malattia che può colpire a tutte le età, e che dipende da un processo infiammatorio di natura "autoimmune" - una specie di processo autodistruttivo, un'aggressione del nostro organismo contro se stesso - che provoca lesioni delle cartilagini e delle estremità ossee. Colpisce circa l'1% della popolazione, un po' più spesso le donne, in genere tra i 25 e i 50 anni. E' una malattia cronica che deve essere riconosciuta precocemente, richiede uno specifico intervento medico e deve essere curata con molta attenzione, pazienza e perseveranza, per ridurre nei limiti del possibile i danni e le sofferenze. Purtroppo, spesso si associa a osteoporosi anche nei giovani e giovanissimi, perché in genere richiede lunghe cure a base di cortisone.
L'artrosi è invece una malattia osteo-articolare determinata da un processo degenerativo. E' più corretto parlare di osteoartrosi, perché oltre alle cartilagini articolari sono sempre interessati anche i capi articolari delle ossa. Si tratta di una malattia frequentissima, che forse colpisce prima o poi, in forma più o meno grave, praticamente tutti coloro che arrivano a una certa età. E' una malattia da usura, nel senso che le articolazioni subiscono un danno che in qualche modo appare legato all'uso, e che si manifesta non improvvisamente, ma con il passare degli anni e dei decenni. Le forme più gravi riguardano spesso categorie particolari di persone, che per vari motivi sottopongono per molti anni le loro articolazioni a stress particolarmente violenti e prolungati. Per esempio, l'artrosi della colonna vertebrale colpisce spesso chi per lavoro fa l'autista, e quindi per molte ore al giorno sta in posizione seduta, trasmettendo direttamente alle vertebre tutte le vibrazioni e le scosse della strada. L'artrosi dell'anca e del ginocchio, forse le forme più invalidanti, sono spesso legate a un forte sovrappeso. L'artrosi del gomito e della spalla è frequente in chi fa per anni lavori manuali pesanti (p.es. chi utilizza mazze, perforatrici, martelli pneumatici). Comunque, come avviene per tutte le malattie, la suscettibilità all'artrosi è individuale, e a parità di "stress", alcuni avranno un'artrosi grave, altri praticamente non ne avranno. L'artrosi non si può "guarire", perché la cartilagine non si rigenera spontaneamente. In genere, la cura dell'artrosi consiste nell'evitare ulteriori peggioramenti e nel ricorso ad analgesici e antinfiammatori contro il dolore (1). Nei casi più gravi e invalidanti, oggi, si può ricorrere a interventi chirurgici che sostituiscono l'articolazione colpita (es. anca) con una protesi artificiale. Si tratta comunque di soluzioni estreme, che non è possibile discutere in questa sede.
Per concludere, possiamo dire che: 1) Chi è in sovrappeso andrà incontro più facilmente all'artrosi, ma almeno in teoria è meno a rischio di osteoporosi. 2) Chi è colpito da artrite reumatoide, sia per la malattia in sè sia per l'uso cronico di certi farmaci ha un rischio aumentato di osteoporosi. In questi casi, sotto la guida del medico, bisogna attuare una precisa strategia di prevenzione dell'osteoporosi. 3) Sfortunatamente, quando si è avanti con gli anni, spesso si soffre contemporaneamente di artrosi e di osteoporosi.
(1) Sottolineiamo a questo proposito che l'uso di questi farmaci (i cosiddetti FANS), anche quando si tratta di prodotti "da banco" in libera vendita, deve essere discusso con il proprio medico. Se il loro uso occasionale è in genere del tutto sicuro, l'uso troppo frequente e prolungato può avere effetti collaterali indesiderati e anche comportare seri rischi.
Principali farmaci contro l'osteoporosi.
I FARMACI CONTRO L'OSTEOPOROSI
Gli estrogeni
Sono i classici farmaci usati - in genere associati o alternati ciclicamente ai progestinici - nella terapia ormonale sostitutiva post-menopausale, e ovviamente sono utilizzabili solo nell'osteoporosi femminile. Agiscono sull'osso riducendo il riassorbimento e determinando una stabilizzazione dei livelli di massa ossea, o anche un piccolo aumento, specie a livello vertebrale. Questo riduce significativamente il rischio di frattura, in particolare delle vertebre. In genere la terapia viene iniziata subito dopo l'entrata in menopausa e deve essere continuata per almeno qualche anno. I suoi effetti continuano per tutta la sua durata. La terapia sostitutiva ormonale aiuta a entrare più dolcemente in menopausa, riducendo alcuni dei disturbi più fastidiosi. Gli estrogeni proteggono non solo l'osso, ma anche riducono anche i tumori intestinali. Invece, determinano un certo aumento del rischio di tumori dell'endometrio (la mucosa interna dell'utero) e soprattutto della mammella, rischio che viene tenuto sotto controllo da opportuni esami periodici in grado di scoprire
eventuali tumori in fase precoce e curabile (Pap-test e mammografia). Gli estrogeni usati per la terapia sostitutiva post-menopausale sono prescrivili a carico del S.S.N. La somministrazione è per via orale o transdermica (cerotti o gel), e la terapia deve essere seguita dal medico con opportuni controlli periodici. Recentemente, le terapie ormonali sostitutive molto prolungate (ben oltre i 5 anni) sono state poste sotto accusa perché i rischi potrebbero superare i benefici. Come per tutte le terapie occorre bilanciare i benefici e i rischi. Durata e posologia della terapia sostitutiva vanno personalizzate in base alle specifiche necessità di ogni singola paziente.
I bisfosfonati
Sono oggi fra i farmaci più usati contro l'osteoporosi. Come gli estrogeni e i SERM, agiscono
sull'osso riducendo il riassorbimento e determinando una stabilizzazione o anche un modesto
aumento dei livelli di massa ossea. Numerosi studi hanno dimostrato che i bisfosfonati sono in
grado di ridurre significativamente il rischio di fratture vertebrali, femorali e periferiche. A differenza
di estrogeni e SERM, riservati alle donne in menopausa, possono essere usati anche nelle forme
di osteoporosi maschile e osteoporosi secondaria a malattie croniche o legata all'uso continuativo
di corticosteroidi. La terapia va iniziata sulla base di una diagnosi di osteoporosi e va assunta a
lungo, in genere senza interruzioni.
I principali bisfosfonati in uso sono: alendronato (per bocca: 10 mg al giorno o 70 mg una volta
alla settimana), risedronato (per bocca, 5 mg al giorno o 35 mg una volta alla settimana),
ibandronato (per bocca, 150 mg una volta al mese), clodronato (generalmente 100 mg per
iniezione intramuscolare, 1 volta ogni 7-15 giorni; la formulazione orale è poco utilizzata). Più di
recente sono entrati in commercio altri 2 farmaci iniettabili, prescrivibili e somministrabili solo in
ospedale, riservati a donne in menopausa con osteoporosi ad alto rischio di frattura: l'ibandronato
(per infusione endovenosa, 3 mg 1 volta ogni 3 mesi) e lo zoledronato (per infusione endovenosa,
5 mg 1 volta ogni 12 mesi). Si tratta di farmaci da riservare ai casi in cui non è possibile assicurare
la continuità delle cure con scadenze più brevi. Infine, sebbene in Italia sia registrato solo per
l'Osteogenesi imperfetta, in caso di difficoltà con i bisfosfonati da prendere per bocca si può usare
anche il neridronato (per iniezione intramuscolare, 25 mg una volta al mese).
I bisfosfonati assunti per bocca si assorbono con difficoltà nell'intestino. Per questo vanno presi
preferibilmente al mattino a stomaco vuoto, meglio se con acqua oligominerale (in particolare,
l'acqua deve essere povera di calcio, perché le acque calcaree riducono l'assorbimento intestinale
di questi farmaci). Dato che i bisfosfonati sono irritanti per la mucosa della bocca e dell'esofago,
devono essere rapidamente deglutiti con un intero bicchiere d'acqua, e dopo l'assunzione non ci si
deve sdraiare per evitare un eventuale reflusso nell'esofago. Per facilitare l'assorbimento non si
devono assumere cibi o altri farmaci per almeno mezz'ora (meglio un'ora) dopo averli presi.
I bisfosfonati per via orale sono controindicati nel caso di patologie esofagee (esofagite, stenosi,
acalasia); di impossibilità di stare a busto eretto per più di 30 minuti; ipocalcemia. Non devono
essere assunti in gravidanza o allattamento: l'uso nelle donne in età fertile è quindi condizionato a
un'efficace contraccezione.
Devono essere assunti con opportune precauzioni nel caso di patologie gastroesofagee (reflusso
gastro-esofageo, disfagia, gastrite, duodenite, ulcera gastrica o duodenale) o se la clearance della
creatinina è minore di 35 ml/min. Fra gli effetti indesiderati sono stati segnalati: esofagite, erosioni
e ulcere esofagee; ulcere gastriche e duodenali; dolore addominale; disturbi della digestione o
della deglutizione; gonfiore addominale; dolori muscolo-osteo-articolari; stitichezza o diarrea;
flatulenza; cefalee. I fenomeni allergici (eruzioni cutanee, eritema, orticaria, edema di labbra,
lingua, faringe) sono rari.
A parte queste avvertenze, i bisfosfonati sono farmaci molto sicuri, ormai sperimentati da molti
anni e usati da milioni di persone in tutto il mondo.
Recentemente ha avuto una certa risonanza sulla stampa la segnalazione di una rara anche se
potenzialmente grave complicanza dell'uso dei bisfosfonati, l'osteonecrosi della mandibola.
Abbiamo ricevuto diverse telefonate allarmate ed è per questo che ne parliamo.
L'osteonecrosi della mandibola è una complicanza molto rara dell'uso dei bisfosfonati. I fattori di
rischio sembrano essere la durata dell'assunzione di bisfosfonati, operazioni chirurgiche odontoiatriche, malattie dentali o periodontali, protesi non adatte, tumori, fumo, uso cronico di corticosteroidi, cattiva igiene orale. Quasi tutti i casi sono stati osservati a seguito di interventi odontoiatrici importanti e coinvolgenti l'osso alveolare (estrazioni dentarie, impianti) in malati di tumori con metastasi ossee, con cattiva igiene orale, trattati con cortisone ad alte dosi e con bisfosfonati ad alte dosi per via endovenosa (essenzialmente zoledronato e pamidronato). I casi riportati in altri tipi di pazienti (malati di osteoporosi o di morbo di Paget osseo) e con bisfosfonati per via orale sono pochissimi (secondo il New England Journal of Medicine del 30 novembre 2006, pag. 2279, meno di 50 casi nell'osteoporosi e meno di 5 nel Paget, su molti milioni di pazienti trattati). L'accurata igiene orale sembra essenziale per la prevenzione. Per massima prudenza, è bene valutare con il medico curante e il dentista l'eventuale sospensione dell'uso di bisfosfonati orali se si rendono necessari importanti interventi odontoiatrici. In tal caso, dopo l'intervento è raccomandato l'uso di antibiotici per almeno 10 giorni. N.B. gli interventi a rischio NON sono le semplici otturazioni, ricostruzioni, copertura con corone dei denti, ma SOLO le estrazioni, gli impianti, e altri interventi che interessano l'osso alveolare della mascella o della mandibola.
Sono una nuova classe di farmaci, la cui sigla sta per "modulatori selettivi dei recettori per gli estrogeni". Si tratta di farmaci che agiscono come gli estrogeni, ma solo a certi livelli. Per esempio, nel caso del raloxifene, (Evista, Optruma)il primo di questa categoria ad essere utilizzato nella terapia dell'osteoporosi, l'azione si esplica a livello dell'osso, ma non di utero e mammella. Il raloxifene inibisce il riassorbimento osseo. In uno studio su oltre 7000 donne dai 31 agli 80 anni, in menopausa da almeno 2 anni e affette da osteoporosi secondo i criteri OMS, che ricevevano supplementi di calcio e di vitamina D, i risultati a 36 mesi sono stati significativamente migliori con il raloxifene che con il placebo sia nel ridurre il numero di nuove fratture vertebrali, sia nell'aumentare la densità ossea. A differenza di un altro SERM, il tamoxifene, usato nella prevenzione delle recidive di carcinoma mammario, il raloxifene non agisce sulla mucosa uterina. Il raloxifene non deve essere usato da donne in età fertile, ma solo da donne in menopausa. Altre controindicazioni all'uso sono: storia di trombosi venosa profonda, embolia polmonare, trombosi venosa retinica; malattie epatiche; sanguinamenti vaginali di natura non chiarita; tumori maligni della mammella o dell'utero. L'assunzione di raloxifene è sconsigliata durante terapia ormonale sostitutiva o altre assunzioni di estrogeni; in persone immobilizzate a letto o in carrozzina; in concomitanza con terapie anti-colesterolo a base di colestiramina. Come tutti i farmaci, il raloxifene può avere degli effetti indesiderati. Sono stati segnalati: eventi tromboembolici venosi profondi (trombosi venosa profonda, embolia polmonare, trombosi venosa retinica) e tromboflebite venosa superficiale; aumentata frequenza di vampate di calore, con comparsa in genere entro i primi 6 mesi di trattamento; crampi alle gambe o edemi periferici (mani, piedi, gambe).
La calcitonina
La calcitonina è stata uno dei primi farmaci disponibili per trattare l'osteoporosi. È stata molto usata negli anni ‘980, ma oggi non è più molto usata. Si tratta di un ormone che produciamo direttamente in cellule specializzate della ghiandola tiroide in condizioni di aumentata disponibilità di calcio nel sangue. La calcitonina va così a bloccare la distruzione dell'osso, che a sua volta libererebbe altro calcio nel sangue. Bloccando il riassorbimento osseo - come abbiamo ricordato sopra - impedisce la progressiva riduzione della massa ossea. La calcitonina non può essere assunta per bocca perché viene inattivata nello stomaco. Si usa preferibilmente per iniezione intramuscolare (è stata studiata anche una forma somministrabile come spray nasale). Gli studi hanno confermato che il farmaco determina un certo aumento della densità ossea e riduce significativamente le fratture vertebrali. Tra gli effetti indesiderati ricordiamo soprattutto sensazione di calore, arrossamento delle orecchie e del volto (subito dopo avere assunto il farmaco), nausea, vomito.
La vitamina D e i suoi derivati attivi
Come abbiamo detto nel capitolo specifico, la vitamina D non è in genere considerata un
"farmaco" perché, in condizioni normali, è normalmente prodotta nel nostro organismo. Tuttavia è
spesso prescritta e usata come "supplemento" per le persone che, come molti anziani, possono
produrne meno del necessario e quindi essere a rischio di carenza. Normalmente si consigliano
supplementi di 400-600 U.I. di vitamina D nativa (colecalciferolo) al giorno, dose che spesso è
abbinata agli integratori di sali di calcio.
I derivati attivi della vitamina D (25-OH vitamina D o calcifediolo; 1,25(OH)2 vitamina D o
calcitriolo; 1-alfa-OH vitamina D o alfacalcidolo) sono equivalenti ai "metaboliti attivi" della vitamina
D prodotti nell'organismo, e sono quindi particolarmente efficaci per migliorare l'assorbimento del
calcio nell'intestino nelle condizioni di carenza di vitamina D.
In particolare negli anziani, in cui la sintesi o l'attivazione della vitamina D possono essere ridotte,
e le carenze sono più frequenti, sono in genere preferibili alla vitamina D nativa. Si tratta di farmaci
molto potenti, che devono sempre essere prescritti dal medico, e usati nella dose corretta.
Prendere dosi troppo elevate, o per troppo tempo, può essere dannoso. Nella terapia a lungo
termine sono necessari regolari controlli su sangue e urine per evitare il rischio di ipercalcemia e
ipercalciuria, e può essere richiesto un aggiustamento dei dosaggi.
Come abbiamo già detto nella pagina dedicata alla vitamina D, è possibile valutare le nostre
"riserve" disponibili misurando il livello di 25-OH vitamina D nel sangue. Se tale livello è inferiore ai
30 ng/ml è indicato un supplemento di vitamina D.
Il paratormone (teriparatide e ormone paratiroideo)
Il paratormone, l'ormone normalmente secreto dalle ghiandole paratiroidi in risposta a uno stato di ipocalcemia (concentrazione troppo bassa di calcio nel sangue), è stato introdotto di recente nella terapia dell'osteoporosi. In commercio in Italia ne esistono due formulazioni: il frammento attivo della molecola del paratormone (chiamato "teriparatide" e ottenuto per sintesi) e la molecola intera. Si tratta tuttavia di un farmaco da usare con estrema cautela e sotto la stretta supervisione di un medico esperto. Il paratormone è il più potente stimolatore del riassorbimento osseo. Attraverso la sua azione si ha una rapida mobilizzazione di calcio dai depositi scheletrici, con un effetto ipercalcemizzante. In realtà, a ogni stimolazione del riassorbimento corrisponde una risposta di neoformazione ossea, per cui il paratormone può essere usato per ottenere ciò che gli altri farmaci finora impiegati non potevano fare: un recupero di massa ossea attraverso lo stimolo alla neoformazione. Tuttavia, a causa dei suoi effetti a doppio taglio, va usato con cautela, solo da parte di specialisti esperti, con opportuni cicli e nei giusti dosaggi, e con regolari controlli del metabolismo osseo. Si usa per iniezione sottocutanea, una volta al giorno, con una speciale penna-siringa a cicli di 6 mesi (ripetibili al massimo per 3 volte, cioè 18 mesi consecutivi). È prescrivile solo da parte di Centri specialistici autorizzati dalle varie Regioni o Province autonome, su piano terapeutico.
Il ranelato di stronzio
E' disponibile in Italia per il trattamento dell'osteoporosi postmenopausale. Lo stronzio è un elemento che ha caratteristiche chimiche simili al calcio: viene assorbito dall'intestino in modo simile al calcio e in parte va a depositarsi sull'osso. Tuttavia il ranelato di stronzio non deve essere considerato un semplice sostituto del calcio, ma un vero e proprio farmaco. Agisce in parte bloccando la fase di distruzione dell'osso e in parte stimolando la fase di formazione, riequilibrando i due processi a favore della formazione. Gli studi clinici hanno evidenziato un recupero di massa ossea e una riduzione del rischio fratture. Il ranelato di stronzio è stato approvato solo per l'uso in donne in menopausa e si prende per bocca una volta al giorno (sono bustine di granutato da sciogliere in acqua), lontano dai pasti. Si consiglia di prenderlo alla sera prima di andare a letto (purché almeno due ore dopo cena). La sua efficacia è stata dimostrata anche in donne anziane, oltre gli 80 anni.
Norme per accesso alla MOC e per la prescrizione dei farmaci con il S.S.N.
Attualmente, le norme per l'accesso alla MOC sono state uniformate in tutte le Regioni italiane, nel
quadro dei "Livelli essenziali di assistenza" (LEA).
La maggior parte dei farmaci oggi riconosciuti come più efficaci contro l'osteoporosi sono
prescrivibili in fascia A - cioè con il solo pagamento del ticket (se applicabile) - secondo la "nota
AIFA 79".
Il medico di famiglia, sulla base delle indicazioni della nota 79, può fare la prescrizione sul normale
ricettario regionale
Source: http://bioactival.it/doc/actitwo/osteoporosi.pdf
Scottish Intercollegiate Guidelines NetworkPart of NHS Quality Improvement Scotland Autism spectrum disordersBooklet for parents and carers We would like to thank all the young people who took part in the focus groups to provide us with their ideas and illustrations for this booklet. © Scottish Intercollegiate Guidelines Network ISBN 978 1 905813 27 8
Scientific report regarding the implementation of the project " Functional diversity of D1 proteins in photosystem II in cyanobacteria" code PN-II-ID-PCE-2011- 3-0765 during January – December 2015 Following the previous stages of the project, the initial phase in 2011, when the project was started, the one in 2012 when the studies on the functional characterization of D1 protein were done, the one in 2013 when studies regarding the functional characterization of D1 protein in different cyanobacteria communities were started and the phase from 2014 when the previous studies have been continued, this year we have done the following activities:







